Inovativni lijekovi pokrivaju više terapijskih područja i troškove, vrijeme i rizike povezane s kandidatima koji ulaze u klinički razvoj znatno se povećavaju. Racionalna strategija istraživanja mora se koristiti, čime se u potpunosti iskorištava postojeće tehnologije, koncentrirajući resurse o kandidatima sa razvojnim potencijalom i eliminirajući one bez održive budućnosti za minimiziranje otpada resursa na projektima.
Ne postoji jednostavan, gotov odgovor o tome kako ublažiti rizike kliničkih razvoja, povećati uspješne stope i ubrzati odobrenje sigurnih i efikasnih lijekova. Nadalje, strategije istraživanja variraju široko na različitim terapijskim poljima. Jedan od najkrhanijih pristupa koristi mehanistički i dokaz-koncept (POC) validaciju u istraživanju ranog stepena. Smjernice 2024 "za ne-kliničke studije adeno povezanih virusa (AAV) vektorskih terapske terapije" također izričito spominju važnost POC-a. Ali šta se tačno potvrđuje kroz POC?
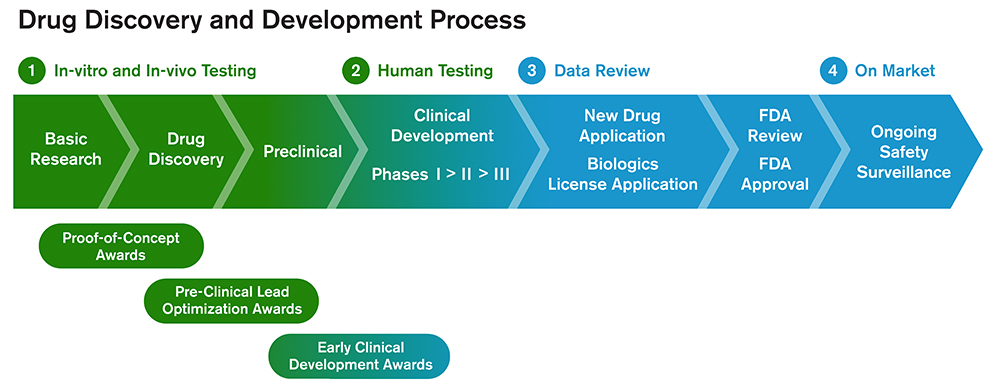
Genske terapije dizajnirane su na temelju dubokog razumijevanja mehanizama bolesti i razvijene su za efikasno izražavanje ciljanih tkiva ili ćelija, vezati se za ciljane web lokacije i modulirati njihovu funkciju kako bi izmijenili progresiju bolesti i rezultiralo u kliničkoj korist. Off-ciljane efekte smatraju se štetnim. Proces se može ukratko opisati u sljedećim koracima: ① Lijek dostiže ciljane ćelije. ② Lijek se izražava u ciljnim ćelijama i veže se na ciljnu stranicu. ③ Ciljna stranica indukuje farmakološki učinak. ④ Ovaj efekat donosi o klinički značajnim promjenama (terapijski ishodi).
Razumijevanje mehanizma djelovanja lijeka rano u razvoju pomaže u vožnji dizajniranju i optimizaciji lijekova, omogućavajući izbor najboljih kandidata za daljnji razvoj. U kasnijim fazama mogu se koristiti metode za provjeru mehanizma djelovanja, postavljanjem temelja za kontinuirani razvoj i na kraju povećavajući brzinu uspjeha i smanjenje rizika.
Predklinički dokaz koncepta (POC)uključujein vitroI studije na životinjama da bi u početku provjerile da li je terapijska strategija AAV-a izvediva, uključujući procjenu efikasnosti i preliminarne sigurnosti. Označava kritičnu tranziciju iz laboratorijskih istraživanja do prekliničkog razvoja (GLP toksikološki studij).
Osnovni ciljevi POC-a
- Valiziranje naučnih hipoteza: Provjera da li AAV vektor može isporučiti ciljni gen, bilo da se izražava u ciljanim tkivima i može li poboljšati fenotipove bolesti.
- Kontrola rizika: Prepoznavanje potencijalnih pitanja (npr. Imunogenost, izvan ciljanih efekata) da bi se smanjio rizik od neuspjeha tokom kasnijeg razvoja.
- Optimizacija: Određivanje optimalnog vektorskog dizajna (serotip, promotor), ruta administracije i raspon doze.
Zašto je POC potreban?
- Naučna validacija: Osigurajte da su strategije uređivanja / zamjene gena efikasne u živim modelima i izbjegavaju lažne pozitive viđene u eksperimentima zasnovanim na stanicama. Potvrdite da AAV-ov ciljanje tkiva odgovara očekivanjima (npr. AAV9-ova sposobnost da pređe krvni mozak barijera).
- Smanjenje razvoja rizika. Poc pomaže na ekranu neefikasne strategije rano.
- Podrška indim aplikacijama: POC podaci su ključna referenca za regulatorne agencije (npr. FDA, EMA) za procjenu obrazloženja iza kliničkih ispitivanja. Nedostatak POC-a mogao bi rezultirati odbijanjem ind.
- Privlačenje investicija: Jasni rezultati POC-a pružaju osnovu za finansiranje i partnerstva, posebno u visoko-cijevnom polju genske terapije.

Kako implementirati POC?
Izbor cilja i modeli bolesti
Mehanizam bolesti: Shvatite da li je to poremećaj jednog gena (npr. HEMOPHILIA) ili multifaktorijalna bolest (npr. Neurodegenerativne bolesti).
Nokaut / mutacijski modeli (npr.,Reumatoidni artritis / cia).
Inducirani modeli (npr.,Steatoza jetre / NASH / MASH).
Validacija modela patologije i sličnosti ljudskim bolestima su od suštinske važnosti.
AAV vektorski dizajn
- Serotip selekcija: Odaberite na osnovu ciljanih tkiva (npr. AAV8 cilja jetre, AVRH10 za CNS).
- Optimizacija promotora: Koristite promotere specifične za tkivo (npr. CTNT za miokard) za poboljšanje ciljanog izražavanja.
- Dizajn transgena: Uključuju kodon optimizaciju i regulatorne elemente (npr. WPRE za poboljšani izraz).
In vitro studije
- Validacija ćelijske linije: Testirajte vektorske efikasnosti transdukcije, nivoa izražavanja gena i toksičnost u hek293 ćelija ili primarnih stanica.
- Analiza izvan cilja: Procijenite nenamjerne izmjene putem RNA-SEQ-a ili sekvenciranja cjelovitih genoma.
- Mala životinja u vivo studijama
- Ruta administracije: Intravensko (sistemsko dostavi), lokalizirano (subretinalno) ili intracerebralno ubrizgavanje.
Oznake efikasnosti
Biomarkers (npr. Povećanje faktora koagulacije IX aktivnosti).
Funkcionalna restauracija (npr. Testiranje čvrstoće mišića, poboljšanja ponašanja).
Histološka analiza (npr. Imunohistohemija za ciljani proteinski izraz).
Istraživanje doze
Testirajte različite doze za određivanje minimalne efektivne doze (MED) i maksimalne tolerirane doze (MTD).
Preliminarna procjena sigurnosti
- Akutna toksičnost:Nadgledajte težinu, aktivnost i serum biohemijske markere (npr. ALT / AST).
- Imunogenost: Procijeniti neutralizaciju antitijela protiv AAV-a i T-ćelijskih odgovora (npr. Ifn-izlučivanje Elispota).
- Vektorska distribucija: Koristite QPCR za procjenu vektorskog DNK u glavnim organima (jetra, srce, mozak, gonade).
Dugoročno praćenje
Monitor monitorskih postojanosti gena (6-12 meseci) i bilo koji potencijalni pad vremenom.
Potražite odloženu toksičnost (npr. Fibroza jetre, rizici formiranja tumora).
Podrška standardima za pretkliničku istraživanje
Objavljene studije Cohena sažeti tri ključna stupa koja podržavaju napredovanje droge kandidata:
- Ciljana izloženost: Lijek mora doći do ciljanog mjesta.
- Ciljna stanarstva: Lijek se mora efikasno vezati na metu.
- Funkcionalna akcija: Lijek mora izazvati funkcionalni učinak na cilju.
Ako su ova tri kriterija ispunjena, verovatnoća uspešnog razvoja lekova je najviša. Ako su samo neki od njih ispunjeni ili nezadovoljni, šanse za uspjeh znatno su smanjene. Za proizvode od terapije Gena AAV-a potrebno je dodatno useljivanje ovih kriterija.
Ključni faktori uspjeha
Značajna poboljšanja krajnjih učinkovitosti na primarnim učinkovitošću (npr. Ekspresija proteina povezanih sa bolestima veći ili jednak 20% normalnog).
Replikacija efikasnosti rezultira najmanje dva modela (npr. Miševi + velike životinje).
Prihvatljiva sigurnost
Nema ozbiljne toksičnosti (npr., Zatajenje jetre, neuroinkalacija).
Kontrolirani imuni odgovori (neutraliziranje naslova antitijela<1:100 or manageable with immunosuppressive pretreatment).
Jasan raspon doze
Uspostavite MTD i MTD i definirajte odnose za odgovor na dozu.
Jasan mehanizam akcije
Potvrdite AAV vektorsku biološku i transgenu izraz u ciljanim tkivima (npr. Koristite u vivo-vivo-oking ili tkivima).
Reproducibilnost i stabilnost
Independent production of AAV vectors in different batches, with consistent results and compliance with preliminary quality control standards (e.g., purity >90%, prazna stopa kapsena<20%).
Razmatranja
Ograničenja životinjskih modela
Modeli glodara ne mogu u potpunosti replicirati ljudske bolesti (npr. Razlike imunološkog sistema), što zahtijeva validaciju s velikim životinjama (svinje,NHP).
Regulatorne varijacije
Smjernice FDA (npr. 2020 "Human Gene terapija za neurodegenerativne bolesti") mogu zahtijevati posebne sigurnosne podatke (npr., Reproduktivna toksičnost).
Procjena resursa
U fazi POC-a, balansiranje dubine istraživanja s troškovima je presudno (npr. Korištenje transgeničkih miševa može biti skuplje od indukovanih modela).
Zaključak
Preklinički POC je osnovna komponenta razvoja terapije AAV-a, koja zahtijeva sistematsku validaciju efikasnosti i sigurnosti tijekom optimizacije parametara liječenja. Kriteriji uspjeha uključuju reproducibilne podatke o učinkovitosti, kontrolirajuće toksičnosti, i jasne odnose odgovora doze, u konačnici postavljaju temelj za inD aplikacije i klinička ispitivanja.












